12月18日,《自然•通讯》(Nature Communications)在线刊出了夏宁邵教授团队发表的题为“Rational design of a triple-type human papillomavirus vaccine by compromising viral-type specificity”的研究论文。基于人乳头瘤病毒(human papillomavirus,HPV)的型别特异性结构基础以及HPV型别分子进化和结构保守性的关系,该研究设计了能够针对三种型别HPV同时产生交叉保护效果的嵌合病毒样颗粒(virus-like particle,VLP),为研发涵盖所有高危型别HPV的更广谱的第三代宫颈癌疫苗奠定了关键技术基础,为多型别病毒疫苗的研制提供了新的思路。

目前已经鉴定出的HPV型别超过200种,分为高危型和低危型。高危型HPV是导致包括宫颈癌在内的多种癌症的主要原因,低危型主要导致尖锐湿疣等疾病。根据世界卫生组织2018年统计数据,世界上每年宫颈癌新发病例约有57万例,死亡病例约31.1万例。在我国每年约有10.6万新发病例,并有约4.8万例死亡病例。研究表明,至少有十三种高危型以及五种可能高危型HPV与宫颈癌等癌症的发生相关。野生型HPV VLP诱导的免疫保护是型别限制性的,无法实现有效的跨型别保护。混合多种型别HPV VLP的多价疫苗是扩大保护范围的主要手段。已上市的宫颈癌疫苗包括二价、四价和九价疫苗,其中保护范围最广的九价疫苗可以预防七种高危型和两种低危型HPV的感染和大约90%的宫颈癌,但仍有与另外近10%宫颈癌相关的HPV没有得到覆盖。随着宫颈癌疫苗的推广应用,疫苗所预防型别的病毒感染将逐渐减少,但疫苗未覆盖型别的病毒传播和进化对人类健康的威胁却可能进一步扩大。因此,有必要研发保护范围更广的宫颈癌疫苗。传统的增加VLP型别进行混合的方法存在着技术上的潜在瓶颈,研制第三代宫颈癌疫苗(HPV二十价)需要另辟蹊径。
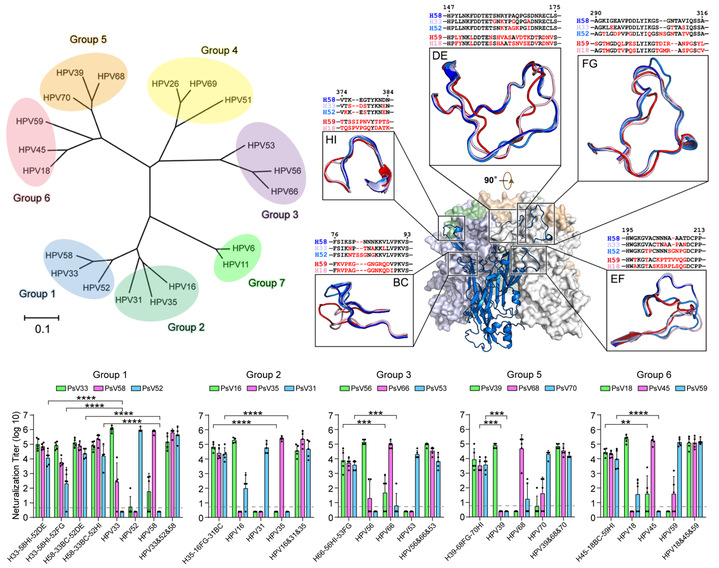
该研究首先分析了二十种型别HPV主要结构蛋白L1的进化关系,并与其中八种型别HPV衣壳粒五聚体晶体结构保守性进行比较,发现型别特异性的优势中和表位是由表面的型别特异性氨基酸和病毒颗粒保守性整体结构共同组成的;利用基于结构信息的同源替换方法,在一种经过分子改造的HPV 58/33/32三型别嵌合VLP上实现了各型别HPV抗原性和免疫原性的平衡,并在非人灵长类动物体内诱导出与3倍剂量的野生型混合VLP相当的交叉免疫保护抗体滴度;进一步利用晶体结构和冷冻电镜(cryo-EM)结构测定揭示了这种嵌合型VLP产生交叉保护的结构基础。该研究还成功地设计出另外的四种三型别嵌合VLP(HPV 16/31/35、HPV 56/66/53、HPV 39/68/70和HPV 18/45/59),验证了这种分子设计策略的通用性,从而为研制七种嵌合VLP保护二十种型别HPV感染的第三代宫颈癌疫苗开辟了新途径。
长期以来,夏宁邵教授团队在HPV疫苗应用和基础研究方面开展了一系列工作。阐明了基于大肠杆菌制备的HPV VLP的组装机制(Structure,2016);研制了即将在国内上市的首个国产第一代宫颈癌疫苗(HPV 16/18双价;Human Vaccines & Immunotherapeutics,2014;Vaccine,2015;Vaccine,2017)、完成二期临床试验的尖锐湿疣疫苗(HPV 6/11双价;Vaccine,2017)和获得临床试验批件的第二代宫颈癌疫苗(HPV九价;Emerging Microbes & Infections,2018);阐明了抗体介导的HPV型别特异性中和作用的结构基础(mBio,2017)。该研究是在深入认识HPV型别特异性的基础上进一步开展的疫苗设计。
我校李智海博士、博士生宋硕和博士生何茂洲为该论文共同第一作者。夏宁邵教授、李少伟教授和顾颖副教授为该论文的共同通讯作者。该研究获得了国家自然科学基金面上项目、国家自然科学基金海峡联合基金项目、新药创制国家科技重大专项的资助。
论文链接:https://www.nature.com/articles/s41467-018-07199-6。
(维多利亚老品牌vic119 欧明展)