肠道病毒是一类在全球广泛流行的小RNA病毒,每年导致超过10亿例新发感染,引发包括呼吸系统、皮肤、神经系统和胃肠道问题等在内的多样疾病。目前已鉴定出300余种血清型,不同型别的流行此起彼伏,且在疫苗的筛选压力下,非主要型别的比例正在上升,新型别的流行也不断出现。因此,无论是对于医疗救护还是疫情防控,均迫切需要监测和鉴定这些肠道病毒型别。现有的肠道病毒分型技术各有局限:病毒中和试验耗时且复杂;基因测序过程缓慢且依赖专业设备和生物信息学分析;核酸杂交技术能够检测更多型别,但敏感性和特异性不及PCR。单管多重PCR提供了相对快速、灵敏的检测方法,但仅能实现3-4个血清型/管的检测,无法满足众多肠道病毒同时鉴定的需求。而设计无相互干扰的引物对在单管超多重检测中极具挑战,且荧光定量PCR仪器的有限检测通道也制约了靶标数的扩展。
针对上述局限,我院夏宁邵、葛胜祥、张师音团队开发了一种序列特异性荧光编码微球(sequence-specific nanoparticle barcode,SSNB)多重核酸检测技术。SSNB技术将靶标特异引物共价偶联至带有不同荧光编码的微球表面,将不同靶标的扩增以颗粒为单位分隔至相对独立的物理空间中,有效避免了常规多重检测中各靶标引物之间、不同靶标引物与模板之间的错配,从而保障了多重扩增的特异性与灵敏度。同时,SSNB技术所采用的微球,最高可实现500种荧光信号编码,每种荧光均可成为该微球表面扩增靶标的唯一编码。通过对微球内部荧光的解码,可判定对应检测靶标属性;而微球表面扩增产物的荧光信号则可指示阴阳性。由此,SSNB在解决传统多重扩增灵敏度与特异性不足问题的同时,亦突破了荧光定量PCR仪检测通道的限制,理论上可实现最高500重的检测。
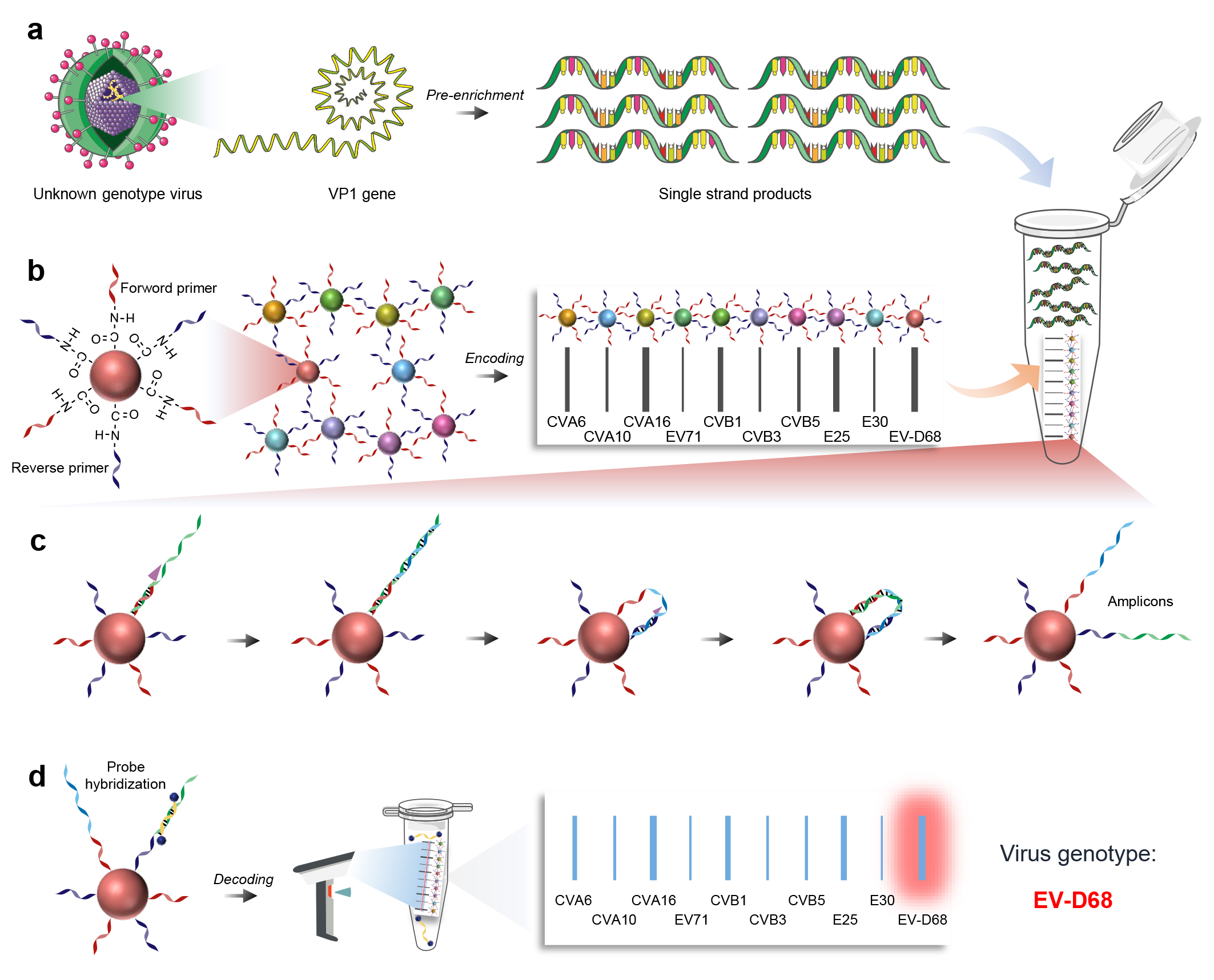
检测原理示意图
基于SSNB技术,研究人员研制出可在一管内对10种高流行的肠道病毒进行分型检测的方法,在型别鉴定中展示出与测序技术100%的一致性,且具备对多型别共感染的鉴定能力。SSNB在提供超多重分析的同时,其呈现出的分析灵敏度显著提升,相比已报道的多重杂交基因分型技术可提升10-10^6倍,临床样本分析中与逐个型别进行分析的单重PCR灵敏度水平相当,并大幅缩短检测耗时并减轻鉴定工作量。作为临床检验工具,SSNB展现出理想的批内及批间可重复性,结果正确可靠。更为重要的是,由于SSNB中每重反应均可形成独立的扩增微环境,不受其他靶标扩增的影响,因此,在需要对新病原进行鉴定时,仅需在体系中补充新引物编码的微球即可,而无需大动干戈式的重新系统调整全部的扩增与检测体系,因此具备更好的靶标拓展性和灵活性。SSNB技术在肠道病毒分型检测中成功应用,验证了其具备理想的敏感性与特异性、超多重检测能力、新靶标拓展能力,以及其无需专业生物信息学分析所带来的便利性。未来,该技术还可应用于症候群病原体鉴定、多基因遗传病检测、肿瘤高频变异基因检测、多耐药位点分析等不同的核酸超多重靶标分析领域,成为核酸多重检测中一种新型的有力工具。
近日,相关研究成果以题为“Sequence-specific nanoparticle barcode strategy for multiplex human enterovirus typing”的研究论文在线发表于《自然·通讯》(Nature Communications)。我院钟泽澄、苏晓崧、杨坤宇为该论文共同第一作者。我院夏宁邵、张师音、葛胜祥为该论文共同通讯作者。该研究得到了国家自然科学基金、福建省科技重大专项、福建省卫生健康委员会医学科研计划项目、中国医学科学院创新单元项目、中央高校基本科研业务费专项资金等项目的支持。
论文链接:https://www.nature.com/articles/s41467-024-50921-w