近日,我院陈洪敏教授团队在国际知名学术期刊Advanced Materials、Advanced Functional Materials、ACS Applied Materials & Interfaces连续发表三篇研究性论文,进一步推动了X射线诱导的光动力肿瘤治疗方向的临床前研究,为该技术的临床转化提供了深厚的理论基础。
众所周知,光学疗法具有侵袭小、副作用小、耐药性小等优点,在临床上被快速发展用于治疗各种肿瘤。然而,激发光的固有浅穿透特性限制了PDT策略的广泛应用。近些年来,联合治疗方法在肿瘤治疗领域快速发展。陈洪敏教授团队利用钆离子(Gd(III))和临床上应用的光敏剂药物孟加拉玫瑰红(Rose Bengal, RB)通过溶剂热反应成功合成了钆-RB配位聚合物纳米点(GRDs)。对比孟加拉玫瑰红前体小分子,GRDs具有独特的吸收特性和7.7倍的显著荧光增强,单线态氧(1O2)生成效率提高了1.9倍。对比常用的磁共振造影剂Gd-DTPA,GRDs的r1弛豫度增加了两倍,同时显示出较强的X射线吸收能力。体外和体内实验结果,证明了GRDs的这些优异性能以及优良的生物相容性和体内安全性。此外,对比单一疗法,GRDs结合了光动力疗法(PDT)和放射疗法(RT),能显着抑制肿瘤的生长,具有广阔的临床转化研究前景。相关研究成果发表于Advanced Materials (2020, 32, 2000377)期刊上。

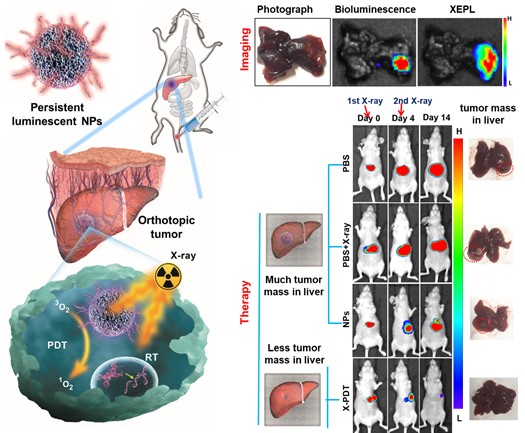
另外一种策略是使用包含闪烁体材料和光敏剂的纳米敏化剂,在相同电离辐射下同时激活PDT和放射疗法(RT),即X射线诱导的光动力疗法(X-PDT)。其中长余辉材料作为一种特殊的闪烁体材料已经引起了生物医学研究者的更多关注。余辉发光不同于普通的荧光材料需要外源光的持续照射产生荧光,而是在终止外源光激发后仍然能够持续发光一段时间,这就避免了生物自发光的存在,可以明显提高信噪比,增强成像的灵敏性和特异性。基于此,课题组采用介孔二氧化硅模板法制备了具有均匀尺寸和单分散球形形貌的mZGGOs长余辉纳米粒子。在低剂量X射线照射下,mZGGOs可发出明显的近红外长余辉光,并且能够穿透1cm肌肉组织在小鼠体内实现有效的余辉成像。通过装载光敏剂,X射线激发的余辉光能够有效激发光敏剂从而杀死癌细胞。体内原位肝癌的余辉成像显示,纳米粒子通过被动靶向机制积聚在肝癌组织中,X-PDT可有效抑制原位肝肿瘤的生长。相关研究成果发表于Advanced Functional Materials (2020, 30, 2001166) 期刊上。
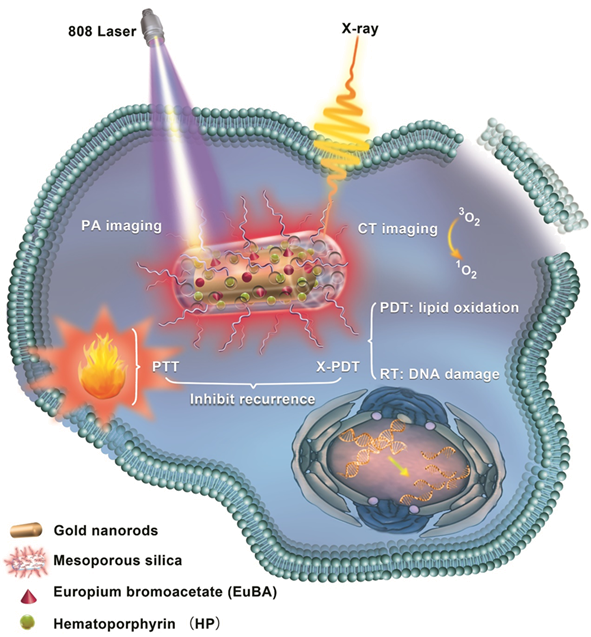
此外,课题组还将光热治疗(PTT)和X-PDT联合,以X射线为激发源的X-PDT与PTT结合能够弥补穿透力的不足;另一方面,PTT可用于抑制DNA损伤修复,增强纳米颗粒在肿瘤中的通透性,增加氧灌注,有利于提高PDT或RT等依赖氧的治疗手段的疗效。我们制备的这种偶联闪烁体和光敏剂的多功能金纳米棒,可以实现CT/PA成像引导下的PTT和X-PDT。通过PTT和X-PDT的联合治疗,一定程度上避免了PTT复发的风险,低剂量的激光和X射线也减少了副作用的危害。镧系配合物闪烁体与金基纳米材料的结合在深部肿瘤的多模态诊疗一体化中具有巨大的潜力。相关研究成果发表于ACS Applied Materials & Interfaces (2020, 12, 12591)期刊上。
我院博士后孙文静博士、硕士生史天航和罗丽分别为论文第一作者,陈洪敏教授和美国国立卫生研究院陈小元研究员均为论文共同通讯作者。该系列研究工作得到了国家自然科学基金、国家重点研发计划、厦门市科技计划和中央高校基本科研业务费专项基金等项目的支持。目前,研究成果已申请中国发明专利2项,正在推动该技术在肿瘤减毒增效治疗方面的临床转化研究。
原文链接:
https://onlinelibrary.wiley.com/doi/10.1002/adma.202000377
https://onlinelibrary.wiley.com/doi/full/10.1002/adfm.202001166
https://pubs.acs.org/doi/10.1021/acsami.0c01189